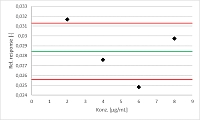
LOD: Wo kommt eigentlich die "3,3" her oder: die zugrundeliegende Statistik

Wer sich schon einmal gefragt hat, warum man die Nachweisgrenze (Limit of detection, LOD) eigentlich mit der Formel
LOD = 3,3 x Standardabweichung / SteigungKalibriergrade
berechnet und wo da die 3,3 eigentlich herkommt, dem mag dieser Beitrag vielleicht ein wenig Licht ins Dunkel bringen.