Interne Qualitätskontrolle, method monitoring und Qualitätsregelkarten
Interne Qualitätskontrolle (QK) – was ist das überhaupt? Sie führen routinemäßig Laboranalysen durch, aber wissen Sie, ob Ihre Methode auch dauerhaft verlässliche Ergebnisse generiert? Ja klar, vor langer Zeit wurde die Methode einmal validiert, aber seitdem…? Können Sie eine Aussage zur Methodenstabilität treffen? Falls sich solche Fragen nicht ganz fremd anhören, möchten wir heute ein Tool vorstellen, was sich genau dieser Thematik zuwendet.
Einführung
Die durchgeführte Validierung der analytischen Methode bildet nur eine Momentaufnahme ab, gibt aber keine Auskunft darüber, ob die Methode auch über die Zeit gesehen wirklich dauerhaft geeignet ist, da der reale Prozess (also unter Berücksichtigung des Faktors „Zeit“) nicht betrachtet wird. Um das zu untersuchen, eignen sich Qualitätsregelkarten, manchmal auch als Kontrollkarten bezeichnet. Diese fallen in das Gebiet der statistischen Prozesskontrolle (SPC, statistical process control). Es gibt verschiedene Arten an Qualitätsregelkarten, welche z.B. in der Normenreihe DIN ISO 7870 beschrieben sind, dazu zählt u.a. auch die Shewhart Qualitätsregelkarte.
Unter interner Qualitätskontrolle ist ein Kontrollprogramm zur kontinuierlichen, kritischen Evaluierung der laboreigenen Analysemethoden zu verstehen. Dies soll sicherstellen, dass die generierten Daten dauerhaft die korrekte Qualität vor dem Hintergrund des beabsichtigten Zwecks der Analysenmethode aufweisen. Das Kontrollprogramm beinhaltet den Einsatz mitlaufender QK-Kontrollproben, die kontinuierliche Eintragung derer Ergebnisse in eine geeignete Qualitätsregelkarte nach Definition geeigneter Warn- und Eingriffsgrenzen sowie einen angemessenen Kontrollrhythmus zur regelmäßigen Überprüfung. Im Englischen wird in diesem Zusammenhang von method (performance) monitoring gesprochen.
Ein Praxis-Beispiel vorweg
Aber bevor wir uns einer Shewhart Qualitätsregelkarte genauer widmen, steigen wir mit einem Beispiel ein. Eine Analysenmethode ist von einem Unternehmen an ein Auftragslabor transferiert worden. Die Methode war schon sehr alt und das Auftragslabor hat daher Optimierungen an der Methode vorgenommen und diese anschließend neu validiert. Bei dieser Methode wurden und werden auch weiterhin parallel zu den eigentlichen Proben bei jeder Analyse QK-Kontrollproben mitlaufen gelassen. Diese QK-Kontrollproben sind auch bekannt als interne Produktkontrolle oder Kontrollmaterial und können z.B. eine speziell für diesen Zweck qualifizierte, ausreichende Menge einer früheren definierten und gut charakterisierten Charge sein oder je nach Probe auch kommerziell erworbenes zertifiziertes Referenzmaterial. Die QK-Kontrollprobe wird genauso behandelt wie die eigentlich zu untersuchenden Testproben. Nach jeder durchgeführten Analyse wird das neue Ergebnis der QK-Kontrollprobe in eine Qualitätsregelkarte eingetragen und der zeitliche Verlauf der Ergebnisse überprüft.
In unserem Beispiel standen zwar genügend historische Daten der QK-Kontrollproben zur Verfügung, doch da die Methode ja optimiert und neu validiert wurde, war nicht klar, ob sich die mit der optimierten Methode zukünftig generierten Werte wie die alten Werte verhalten würden und daher die mit den historischen Werten aufgesetzte Qualitätsregelkarte weiterhin passend sein würde…
Die Hintergründe: Normalverteilung
Nachdem wir uns das jetzt gut praktisch vorstellen können, sollten wir jedoch etwas weiter ausholen, um die Hintergründe zum Aufbau der Qualitätsregelkarte und somit auch obige Problematik auch zu verstehen. Wie wir alle noch aus Schulzeiten wissen, gibt es unter den quantitativen (auf einer Skala messbaren) Daten solche, die normalverteilt sind und solche, die das nicht sind.
Für die Anwendung der hier beschriebenen Qualitätsregelkarte müssen die Daten normalverteilt vorliegen, also der typischen Gaußschen Glockenkurve folgen (siehe folgende Abbildung). Das liegt daran, dass die hier später beschriebene Shewhart Qualitätsregelkarte in ihrem Aufbau auf den Prinzipien der Normalverteilung fußt. Aber wie war das nochmal genau mit der Normalverteilung?
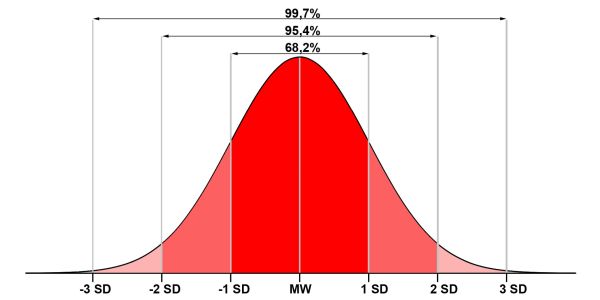
Die Gaußsche Glockenkurve (Häufigkeitskurve) veranschaulicht die relative Häufigkeit einer Merkmalsausprägung in einem unendlich großen Datensatz. Bei normalverteilten Daten, wie hier in der Glockenkurve gezeigt, schwanken die Einzelwerte des Datensatzes um den Mittelwert (MW; Anm. d. Red.: Korrekterweise müsste ich eigentlich vom Erwartungswert µ sprechen… aber aus Vereinfachungsgründen bleiben wir beim Mittelwert, da besser vorstellbar.). Die Schwankung wird über die Standardabweichung (SD) ausgedrückt. Im Bereich von -1 bis +1 Standardabweichung sind ca. 68% aller Werte des Datensatzes enthalten, zwischen -2 SD und +2 SD bereits ca. 95% und wenn man die Spanne von der dreifachen Standardabweichung in beide Richtungen berücksichtigt, werden ca. 99% aller Ergebnisse abgedeckt.
Der Aufbau der Shewhart Qualitätsregelkarte
Und wer sich jetzt fragt, warum dieser Ausflug in die Normalverteilung wichtig war, dem sei gesagt, dass wir für Erstellung einer Shewhart Qualitätsregelkarte auch die Informationen zum Mittelwert und zur Standardabweichung des uns interessierenden Datensatzes brauchen.
Die Shewhart Qualitätsregelkarte ist eine anschauliche Grafik, bei der auf der x-Achse der zeitliche Verlauf betrachtet wird und auf der y-Achse die Merkmalsausprägungen eingetragen werden. Dazu kommen nun als gerade horizontale Linien die 2SD- und 3SD-Werte, welche als Schranken fungieren. Dabei wird die 2SD-Linie als Warn- und die 3SD-Linie als Eingriffsgrenze bezeichnet. Zwischen diesen Grenzen dürfen sich die Werte bewegen. Auch wenn die Verwendung von 2SD und 3SD für die Warn- und Eingriffsgrenzen am häufigsten ist, können natürlich auch je nach Merkmal auch andere Grenzen verwendet werden.
In einem „Vorversuch“ werden anhand einer bestimmten Anzahl an Daten aus der Vergangenheit (wenn wir an obiges Beispiel der Labormethode denken, so waren das die „historischen Daten“) der Mittelwert und die Standardabweichung bestimmt. Dabei gilt grundsätzlich, je mehr Daten, desto stabiler werden die sich aus der Standardabweichung abgeleiteten Grenzen. In [1] werden für den Start ungefähr 25 Werte empfohlen, welche auch auf den Ergebnissen der Methodenvalidierung beruhen können.
Aber veranschaulichen wir uns die Konstruktion und den Aufbau einer Qualitätsregelkarte am besten mit Hilfe eines Beispiels. Wir haben folgende historische Daten der QK-Kontrollprobe einer Gehaltsbestimmung von Tabletten (in diesem Beispiel: 20 untersuchte Chargen):
| Gehalt [mg] | Statistische Kenndaten [mg] | |
| 1 | 399 |
Mittelwert: 398,8 SD: 5,3
2SD 10,7 3SD 16,0
Untere Warngrenze (UWG): MW – 2SD = 388,1 Untere Eingriffsgrenze (UEG): MW – 3SD = 382,8 Obere Warngrenze (OWG): MW + 2SD = 409,5 Obere Eingriffsgrenze (OEG): MW + 3SD = 414,8
|
| 2 | 393 | |
| 3 | 402 | |
| 4 | 394 | |
| 5 | 405 | |
| 6 | 397 | |
| 7 | 395 | |
| 8 | 401 | |
| 9 | 394 | |
| 10 | 392 | |
| 11 | 406 | |
| 12 | 407 | |
| 13 | 390 | |
| 14 | 397 | |
| 15 | 405 | |
| 16 | 399 | |
| 17 | 392 | |
| 18 | 405 | |
| 19 | 403 | |
| 20 | 400 |
Mit diesen Zahlen konstruieren wir jetzt die vorläufige Qualitätsregelkarte: In ein Diagramm mit dem zeitlichen Verlauf auf der x-Achse und der Merkmalsausprägung auf der y-Achse (hier: Gehalt in mg) zeichnen wir als horizontale Linien ganz unten bei 382,8 mg die UEG in rot, bei 388,1 mg die UWG in grün, bei 409,5 mg die OWG in grün und bei 414,8 mg die OEG in rot als entsprechende 2- bzw. 3SD-Grenzen ein. Die dazwischen liegenden Bereiche sind dann der entsprechende Warn- bzw. Eingriffsbereich. Das sieht dann so aus:
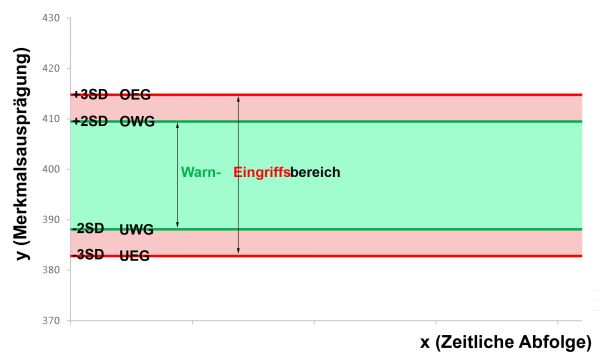
Im Falle historischer Daten mit vermutlichen Ausreißern wird in [2] die Anwendung von robusten Schätzverfahren empfohlen. Des Weiteren ist nach einem bestimmten, längeren Zeitraum zu prüfen, ob die mit den historischen Anfangsdaten erzeugte Qualitätsregelkarte für die Praxis geeignet ist. Zur finalen Festlegung der Grenzen wird in [1] ein Zeitraum von einem Jahr und mindestens 60 Werten empfohlen. Aber auch für den Zeitraum danach sollte firmenintern definiert sein, in welchen Abständen eine Re-Evaluierung der Kontrollgrenzen stattfinden sollte.
Zweck und Anwendungsmöglichkeiten für Qualitätsregelkarten
Nachdem wir jetzt gesehen haben, wie eine Qualitätsregelkarte aufgebaut ist, sollten wir an unser Anfangsbeispiel denken, womit wir zur Frage kommen, welchem Zweck solche Qualitätsregelkarten dienen. Obiges Beispiel deutet es schon an: die regelmäßige Eintragung unserer analytischen Ergebnisse der QK-Kontrollprobe nach jeder durchgeführten Analyse in eine Qualitätsregelkarte hilft, zeitabhängige Veränderungen frühzeitig zu erkennen. Mit ihr überwachen wir den Einfluss systematischer und zufälliger Fehler auf unsere Analysenmethode. Spontane Abweichungen vom üblichen Verlauf werden durch Überschreitungen der Warn- oder Eingriffsgrenze auf einen Blick erkannt.
Dabei ist es durchaus ok, wenn mal ein Wert zwischen der Warn- und Eingriffsgrenze liegt, da wir mit ± 2 SD (für den Warnbereich) ja nur 95% aller Ergebnisse abdecken, also 5% auch mal „außen vor“ sein können… Wenn jedoch ein Wert außerhalb der Eingriffsgrenze liegt (was ja nur bei 3 von 1000 Messungen eintritt) kann man mit sehr hoher Wahrscheinlichkeit davon ausgehen, dass diese Analyse fehlerhaft war. Aber auch schon bevor es zu einer Überschreitung einer Warn- oder Eingriffsgrenze kommen mag, können z.B. auch Trends (= gerichtete Häufungen) erkannt werden, wenn sich zwar alle Daten noch im normalen Bereich aufhalten, aber die Werte beispielsweise chronologisch zunehmend niedriger werden… Oder wenn auf einmal eine ungewohnt hohe Variabilität in den Daten zu sehen ist, die vorher so nicht da war… Das sollte einem zu denken geben! Irgendwas stimmt da nicht mehr. Aber da denken allein nicht reicht, sollte man natürlich auch der Ursache auf den Grund gehen 😉 Eine mögliche simple Erklärung könnten z.B. eingesetzte, gealterte Reagenzien sein…
Wir bleiben bei unserer Gehaltbestimmung von Tabletten und schauen uns die folgenden zwei Szenarien an. Wir haben jeweils 20 Ergebnisse der mitgelaufenen QK-Kontrollprobe und der Mittelwert liegt bei beiden genau bei 400 mg und die Standardabweichung jeweils bei 4,7 mg. Diese Zahlen sagen erstmal gar nichts. Ohne eine Visualisierung in Form einer Qualitätsregelkarte könnte man naiv denken, dass sich beide gleich verhalten. Wenn wir uns jedoch den jeweiligen zeitlichen Verlauf ansehen, stellen wir fest, dass bei Szenario A alles in Ordnung ist, da alle Werte rund um den Mittelwert mal nach oben und mal nach unten herum schwanken. Anders sieht es aus bei Szenario B: Hier ist eindeutig ein abnehmender Trend zu erkennen!
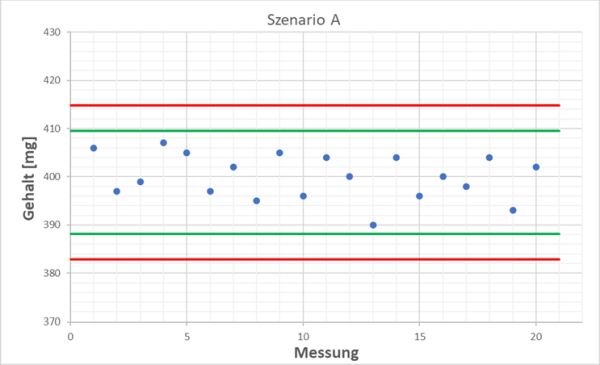
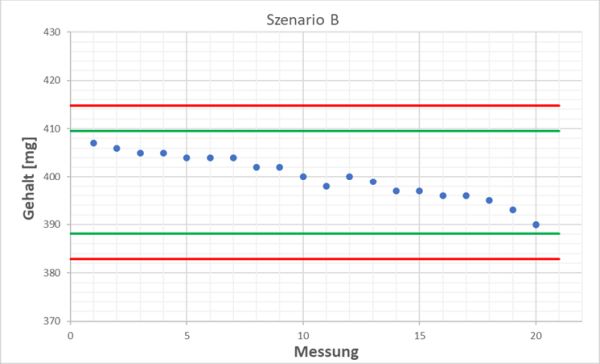
Mit der Führung einer Qualitätsregelkarte haben wir also jederzeit die Performance unserer analytischen Methode im Blick (Stichwort: „Method Performance Monitoring“ oder „Ongoing Monitoring“). Aber nicht nur der reine Messwert der QK-Kontrollprobe, sondern z.B. auch SST-Kriterien, die Wiederfindung einer gespikten Positivkontrolle oder Kalibrierparameter wie Steigung oder Achsenabschnitt können mit Hilfe einer Qualitätsregelkarte im Auge behalten werden.
Außer bei der eigentlichen Analysenmethode können Qualitätsregelkarten z.B. auch im Rahmen der Prüfmittelüberwachung beim arbeitstäglichen, morgendlichen Prüfen der Analysenwaage(n) oder von Pipetten zum Einsatz kommen. Und wenn wir über den Tellerrand blicken, so macht der Einsatz von Qualitätsregelkarten insbesondere bei Prozessparametern wie z.B. der Füllmenge bei Abfüllprozessen in der pharmazeutischen Industrie oder der Lebensmittelindustrie besonders Sinn. In diesen Fällen ist es sinnvoll, anstelle der 2- oder 3fachen Standardabweichungen definierte Sollwerte als Grenzen zu verwenden.
Gemäß [1] können die Ergebnisse einer Qualitätsregelkarte je nach Typ und verwendeter QK-Kontrollprobe z.B. auch zur Ermittlung der Messunsicherheit, zum Methodenvergleich, zur Abschätzung der Nachweisgrenze (nicht unbedingt im Pharma-Bereich) oder zur Bewertung von Ringversuchen Anwendung finden.
Natürlich muss firmenintern auch der Umgang mit den zu beobachtenden „Unregelmäßigkeiten“ (Abweichungen, Variabilität, Trends) geregelt sein. Sprich:
- Was ist zu unternehmen, wenn etwas beobachtet wird?
- Wie wird auf welchen Fall reagiert?
- Was macht man, wenn man „nur“ einen singulären Abweichler hat, der sich zwischen der Warn- und Eingriffsgrenze befindet? Was, wenn er außerhalb ist?
- In welchen Fällen spricht man davon, dass die Methode statistisch bei der Langzeitauswertung außer Kontrolle ist, wenn z.B. 6 [2] oder 7 [1] konsekutive Werte stetig abfallen oder zunehmen oder x aufeinanderfolgende Werte auf derselben Seite des Mittelwerts liegen?
Abschließend ein paar regulatorische Worte
Auch wenn im EU GMP Leitfaden im Kapitel 6 zur Qualitätskontrolle nicht explizit von der Verwendung von Qualitätsregelkarten gesprochen wird, finden sich jedoch Hinweise, dass analytische Testergebnisse auch hinsichtlich Trends untersucht werden sollten [3], wofür sich ja der Einsatz von Qualitätsregelkarten anbietet.
Anders sieht das im Hinblick auf die Steuerung des Produktionsprozesses aus. Hier macht das deutsche Aide-mémoire der Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten (ZLG) zur Inspektion der Validierung von Herstellprozessen (AiM 07122901) einen Exkurs in u.a. die statistische Prozesslenkung und erläutert dabei auch Qualitätsregelkarten [4]. Ebenso wird in der ICH Guideline zum Risikomanagement Q9(R1) im Anhang I.9 auf den Einsatz von u.a. Qualitätsregelkarten als unterstützenden statistischen Werkzeugen für das Qualitätsrisikomanagement hingewiesen [5].
Um den Bogen wieder zurück zu einem Labor der Qualitätskontrolle zu spannen, sei ein Blick in die DIN EN ISO/IEC 17025:2018 geworfen. Diese ist im Vergleich zum Kapitel 6 des EU GMP Leitfadens deutlich konkreter, da sie in Abschnitt 7.7 zur Sicherung der Validität von Ergebnissen die Anwendung statistischer Techniken zur Überwachung der analytischen Ergebnisse im Hinblick auf Tendenzen und auch die Ergreifung geeigneter Maßnahmen bei Werten außerhalb definierter (Eingriffs)Kriterien fordert. Des Weiteren wird hinsichtlich der Prüfmittelüberwachung der Einsatz von Regelkarten erwähnt [6].
Im Zuge der neueren Entwicklungen des Analytical Procedure Lifecycle Konzeptes wird ein kontinuierliches Monitoring der analytischen Methode in der ICH Q14 empfohlen [7] sowie im Kapitel <1220> des amerikanischen Arzneibuchs (USP) inklusive der Anwendung von Qualitätsregelkarten gefordert [8].
Zusammengefasst sei gesagt, dass je nach regulatorischer Umgebung des Labors der Einsatz von Qualitätsregelkarten nicht in jedem Fall erforderlich sein mag, aber durchaus Sinn macht und zunehmend Beachtung findet.
Referenzen
[1] Magnusson B., Hovind H., Krysell M., Lund U., Mäkinen I. (2018). Handbook of Internal Quality Control, Nordtest Report TR 569 (edition 5.1)
[2] Ellison S.L.R., Barwick V.J., Duguid Farrant T.J. (2009). Practical Statistics for the Analytical Scientist: A Bench Guide, 2nd edition, RSC Publishing, ISBN: 978-0-85404-131-2
[3] European Commission (2014) “EU Guidelines for Good Manufacturing Practice for Medicinal Products for Human and Veterinary Use”
[4] Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten (2017) „Inspektion der Validierung von Herstellprozessen (Prozessvalidierung)“ (AiM 07122901)
[5] International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use (ICH) (2023) “Quality Risk Management” Q9(R1)
[6] DIN EN ISO/IEC 17025:2018
[7] International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use (ICH) (2023) “Analytical Procedure Development” Q14
[8] United States Pharmacopoeia, USP-NF (2022) <1220> “Analytical Procedure Life Cycle”
