Methodenoptimierung zur Erhöhung der Sensitivität bei LOQ/LOD-Problemen
In unserem ersten Blogbeitrag zur Erhöhung der Sensitivität bei LOD/LOQ-Problemen bei HPLC-Methoden haben wir die Erhöhung der Sensitivität vorwiegend durch die Reduktion des Basislinien-Rauschens behandelt. Nun betrachten wir dasselbe Thema aus der Sicht der Methodenoptimierung. Was kann an einer Methode optimiert werden, um die Peakhöhe zu steigern und damit das Signal-Rausch-Verhältnis zu verbessern?
In diesem Blogbeitrag sorgen wir uns nicht um außerplanmäßige Probleme wie Lecks, Verunreinigungen, Druckschwankungen oder durch Alterung der Säule entstehende Veränderungen in der Peakform. Wir gehen davon aus, dass die betrachtete Methode gut etabliert und robust ist und lassen daher die üblichen Troubleshooting-Themen hinter uns.
„Peakschärfung“ durch Gradientenläufe
Die Höhe eines Peaks hängt von verschiedensten Faktoren ab. Ein direkter Zusammenhang besteht zwischen der Höhe und der Breite eines Peaks: Ein breiter, flacher Peak kann dieselbe Area besitzen, wie ein schmaler, hoher Peak. Während der breite Peak jedoch bei den Vorgaben zum Signal-Rausch-Verhältnis durchfallen kann, stehen die Chancen für den schmalen viel höheren Peak deutlich besser. Grundsätzlich sollte zunächst ein Blick auf die Grundlagen der Methode geworfen werden. Handelt es sich um einen Gradienten (zum Beispiel von 0% Wasser zu 100% Acetonitril) oder ein isokratisches Programm (durchgehend 50% Acetonitril beispielsweise)? Ein isokratisches Programm hat den Vorteil, dass man am Ende eines Laufs die Säule nicht umspülen muss und so Zeit und Lösungsmittel sparen kann. Der Nachteil ist, dass die Peaks oft breiter sind als bei Gradientenläufen. Reicht das Signal-Rausch-Verhältnis also nicht aus, lohnt sich die Umstellung auf einen Gradienten. Ein Lösungsmittelgradient führt zur „Schärfung“ der Peaks, also zur Verschmälerung und damit auch zur Erhöhung.
Es bleibt jedoch zu beachten, dass nicht jeder Gradient ideal verwendet wird. Ist beispielsweise die Retentionszeit unseres Peaks sehr hoch, kann durch eine Streckung des Gradienten nicht nur die Retentionszeit, sondern auch die Peakbreite reduziert werden. Betrachten wir dies anhand der Umkehrphasen-HPLC (Reversed phase, RP). Wir verwenden einen linearen Gradienten von 100% Wasser (polar) zu 100% Acetonitril innerhalb von 45 Minuten. Wir stellen dabei fest, dass unser Analyt erst bei etwa 80% Acetonitril von der Säule eluiert (siehe erste Abbildung: Ursprungsmethode). Wenn die Probenzusammensetzung nicht allzu komplex ist, lohnt sich hier eine Kürzung des Gradienten von 60% Acetonitril auf 100% Acetonitril in beispielsweise 15 Minuten (siehe erste Abbildung: eingeschränkter Gradient). So haben wir eine kürzere Analysenzeit, schärfere Peaks und eine kürzere Umspülzeit, da wir nicht von 100% Acetonitril auf 0% sondern auf 60% umspülen müssen. Ist die Einschränkung des Gradienten schwierig, da wir mehrere Analyten unterschiedlicher Polarität trennen wollen, kann man versuchen, den Gradienten „steiler“ zu fahren, d.h. wir behalten den Gradienten von 0% auf 100% Acetonitril, verkürzen aber die Analysenzeit von 45 Minuten auf 20 Minuten (siehe erste Abbildung: steilerer Gradient). Wichtig ist hierbei, dass dennoch alle Analyten gut getrennt bleiben.
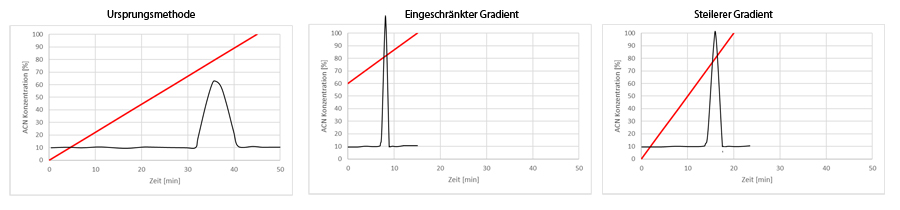
Bei einfachen Analysen mit sehr wenigen Probenbestandteilen kann man noch einen Schritt weitergehen und eine kürzere Säule verwenden, um kürzere Retentionszeiten zu erlangen.
Die Säulenparameter als Einflussgröße
Ist ein langer, flacher Gradient notwendig, um alle Analyten voneinander zu trennen, hilft ein Blick auf die Säulenparameter: Die Annahme, je länger eine Säule, desto bester ist die Auflösung, ist zwar grundsätzlich nicht falsch – dennoch haben Partikelgröße und der Innendurchmesser der Säule oft einen viel stärkeren Einfluss sowohl auf die Auflösung als auch auf die Peakbreite und -höhe. Vergleicht man zwei Säulen gleicher Länge, so kann durch die Verringerung des Säulendurchmessers von 4,6 mm auf 3 mm die Peakhöhe auf das 5-fache erhöht werden während gleichzeitig die Auflösung verbessert wird. Doch aufgepasst: Verwendet man für beide genannten Innendurchmesser dieselbe Flussrate (mL/min), so steigert sich die Fließgeschwindigkeit (auch linear velocity, z.B. cm/min) mit sinkendem Innendurchmesser. Wird die Fließgeschwindigkeit zu hoch, äußert sich das in einem zu hohem Rückdruck und verschlechterter Auflösung und Sensitivität. Für jede Säule gibt es ein Effizienzmaximum bezogen auf die Flussrate, hier sollte man einen Blick in die Herstellerangaben werden, um Einbußen bei der Trennung zu vermeiden. Skaliert man die Flussrate entsprechend so, dass die Fließgeschwindigkeit beider Säulen dieselbe ist, wird man feststellen, dass sogar die Retentionszeiten ähnlich sind, während man Sensitivität, Auflösung und Lösungsmittelverbrauch reduziert hat.
Besonders bei „sauberen“ oder zuvor aufgereinigten Proben lohnt sich außerdem die Umstellung auf eine kleinere Partikelgröße, um die Auflösung weiter zu steigern. Zu beachten ist hier, dass bei gleicher Säulenlänge der Rückdruck mit sinkender Partikelgröße deutlich ansteigt. Die Verringerung der Partikelgröße kann oft sehr gut mit der Verwendung einer kürzeren Säule verwendet werden, wodurch der Rückdruck wieder sinkt. Mit dieser „Minimalisierung“ des Systems kann eine Methode effizient optimiert werden: Die verkürzte Säule hat im Vergleich zu einer längeren Säule eine schlechtere Auflösung. Dies wird ausgeglichen durch die Verwendung kleinerer Partikel und einem kleineren Innendurchmesser, die für eine bessere Sensitivität und Auflösung sorgen (siehe Abbildung):
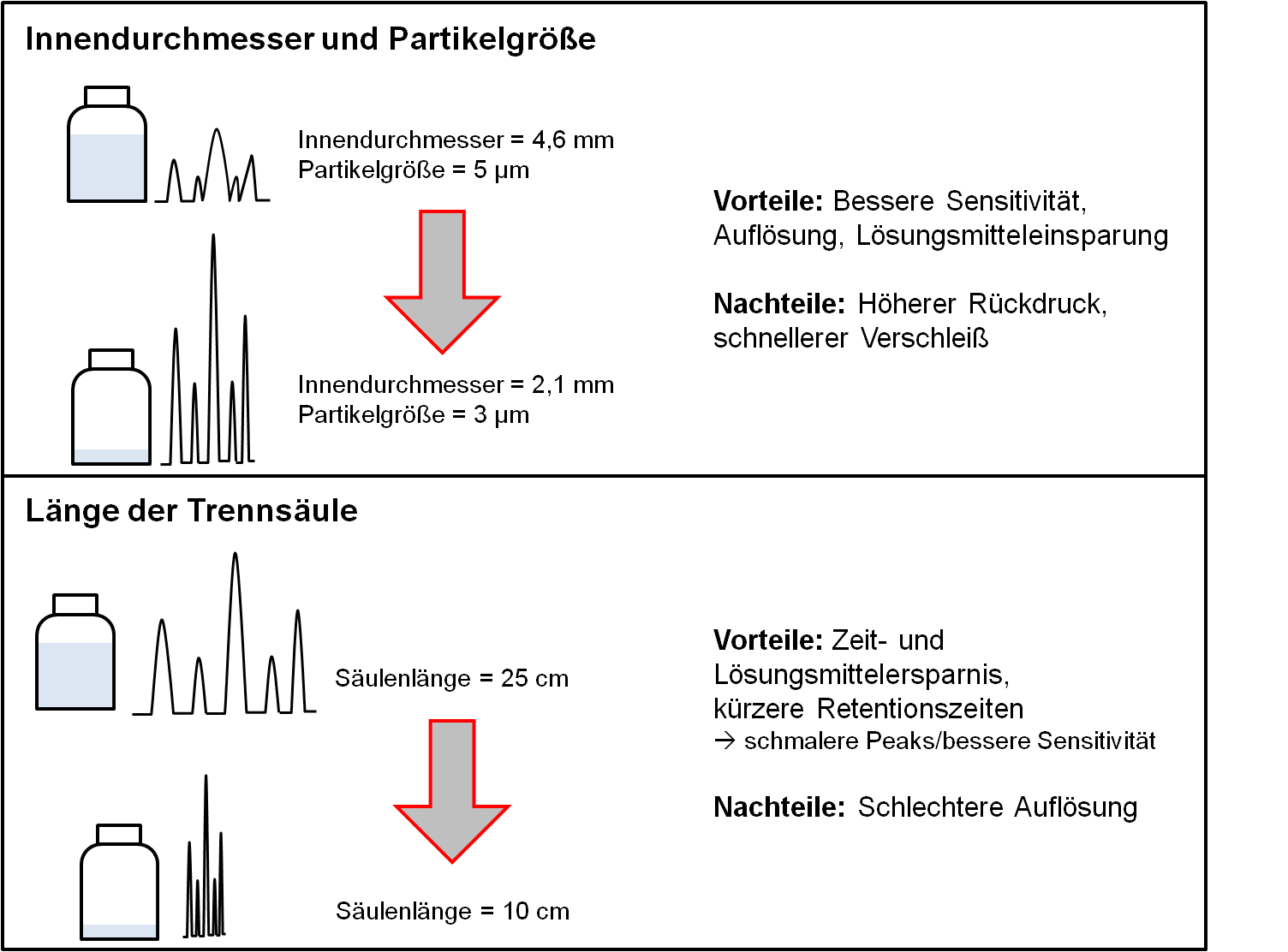
Wird die Fließgeschwindigkeit beibehalten (durch entsprechende Verringerung der Flussrate), kann durch Umstellung einer 25 cm langen Säule mit 5 µm Partikeln und einem inneren Durchmesser von 4,6 mm auf eine 12,5 cm langen Säule mit 3 µm Partikeln und innerem Durchmesser von 2,1 mm die Peakhöhe um ein Vielfaches gesteigert werden (durch kleinere Partikel und Innendurchmesser), während die Retentionszeit halbiert werden kann (durch Halbierung der Säulenlänge). Je nach Komplexizität der Probe kann mit der Länge der Säule die Auflösung verbessert werden. Hier lohnt sich auch ein Blick auf die sogenannten Core-Shell Säulen: Während herkömmliche Silikatpartikel unregelmäßig und vollporös sind, besitzen Core-Shell Partikel einen undurchlässigen Kern („Core“) mit gleichmäßiger Größe. Dieser Kern ist von einer porösen Hülle (daher „Shell“) umgeben, mit dem die eigentlichen Wechselwirkungen stattfinden. Durch die gleichmäßige Partikelgröße ist eine geordnetere Packung der Säule möglich, was zu geringeren Drücken führt. Die Verwirbelung und Diffusion der Analyten ist durch die geringere Tiefe der Hülle im Vergleich zu vollporösen Partikeln deutlich reduziert, wodurch die Analyten in schmaleren Peaks und oft auch kürzeren Retentionszeiten eluieren.
Nachteil von Core-Shell Säulen, aber auch von sehr klein dimensionierten Säulen ist die geringere Ladekapazität und eine höhere Sensitivität gegenüber starken Probenlösungsmitteln (siehe auch unseren Blogbeitrag zu Peakverbreiterung und Fronting/Tailing). Als Folge kann eine Verdünnung der Probe und/oder der Wechsel des Probenlösungsmittels nötig sein.
